Morinaga Milk recibe el registro de "nuevo ingrediente alimentario" en China por el uso de su probiótico Bifidobacterium infantis M-63 en alimentos infantiles
Morinaga Milk recibe el registro de "nuevo ingrediente alimentario" en China por el uso de su probiótico Bifidobacterium infantis M-63 en alimentos infantiles
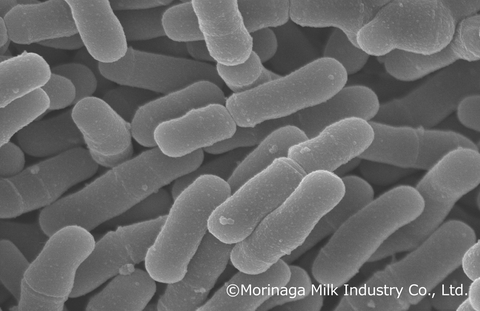
Bifidobacterium infantis M-63 is a unique probiotic strain of human-residential bifidobacteria (HRB) – bifidobacteria that naturally reside in the human gut – and is renowned for its ability to utilize human milk oligosaccharides (HMO) found in breast milk, significantly improving the intestinal environment of healthy full-term infants. (Graphic: Business Wire)
TOKIO--(BUSINESS WIRE)--Morinaga Milk Industry Co., Ltd. (TOKIO:2264), empresa japonesa líder en productos lácteos, anunció hoy que su probiótico patentado Bifidobacterium infantis M-63 fue aprobado por la Comisión Nacional de Salud (NHC) de la República Popular China como nuevo ingrediente alimentario para emplearlo en alimentos para bebés y niños (menores de tres años) el 25 de julio de 2024. Se trata de un hito muy importante para la empresa, ya que la convierte en la única firma japonesa que cuenta con tres cepas de bifidobacterias registradas para el mercado chino de alimentos para bebés y niños pequeños1 .
*1 Fuente: Anuncio publicado en el sitio web del Centro Nacional de Evaluación de Riesgos para la Seguridad Alimentaria de China, el 5 de agosto de 2024.
La cepa Bifidobacterium infantis M-63, que fue la última aprobada, se suma a las otras cepas aprobadas de Morinaga Milk, Bifidobacterium breve M-16V y Bifidobacterium longum BB536. Las tres cepas ya se encuentran autorizadas para aplicarlas en alimentos para niños menores de tres años en China, cumpliendo las estrictas normas nutricionales y de seguridad del país.
Amplía su presencia mundial
Esta aprobación responde a la visión a 10 años de Morinaga Milk, por la cual planea convertirse en una empresa de renombre mundial, con una importante presencia internacional. Como parte de esta visión, la empresa tiene como objetivo alcanzar un ratio de ventas Global Business del 15 % o superior para el año fiscal que finaliza en marzo de 2029. La aprobación de Bifidobacterium infantis M-63 representa un paso estratégico en pos de ese objetivo, y le permite a Morinaga Milk consolidar su negocio de bacterias en el mercado chino, que representa más del 40 % del mercado mundial de leche de fórmula y es el segundo mercado mundial de suplementos2 .
*2 Fuente: Encuesta de Euromonitor International, realizada en mayo de 2024, basada en los precios de venta al por menor
Beneficios para la salud de Bifidobacterium infantis M-63
Bifidobacterium infantis M-63 es una cepa probiótica exclusiva de bifidobacterias residenciales humanas (HRB) -bifidobacterias que se alojan de forma natural en el intestino humano, conocida por su capacidad para utilizar los oligosacáridos de la leche humana que se encuentran en la leche materna, con lo cual mejora significativamente el entorno intestinal de los lactantes sanos nacidos a término. Habiéndose aprobado en China el uso de estos oligosacáridos en la leche de fórmula en octubre de 2023, 3 , se estima que la combinación de Bifidobacterium infantis M-63, Bifidobacterium infantis M-63 y estos oligosacáridos, favorezca el crecimiento de las bacterias intestinales beneficiosas, mejorando el desarrollo y la salud de los lactantes y los niños pequeños4 .
*3 Fuente: Comisión Nacional de Salud de la República Popular China, n.º 8, 2023 (22 de septiembre de 2023)
*4 Fuente: Mintel, "HMOs approval in China infant formula is a game changer" (enero de 2024)
Cepas probióticas de bifidobacterias registradas como nuevos ingredientes alimentarios en China |
|
Cepa |
Fecha de registro |
Bifidobacterium breve M-16V Nombre registrado: 短双歧杆菌 M-16V |
2016 |
Bifidobacterium longum subsp. longum BB536 Nombre registrado: 长双歧杆菌长亚种 BB536 |
2022 |
Bifidobacterium longum subsp. infantis M-63 Nombre registrado: 长双歧杆菌婴儿亚种M-63 |
2024 |
* Estas tres cepas ya han sido aprobadas para alimentos para lactantes y niños menores de tres años. |
|
Compromiso con la calidad y la investigación
Morinaga Milk está a la vanguardia de la investigación sobre bifidobacterias desde su descubrimiento de la Bifidobacterium longum BB536 en 1969. La empresa es líder mundial en cuanto al número de trabajos de investigación clínica sobre las bifidobacterias, demostrando así su compromiso con el avance de la comprensión científica y la mejora de la salud pública.
Perspectivas para el futuro
El hecho de haber registrado a la Bifidobacterium infantis M-63 abre el camino para su uso en una amplia gama de productos. Morinaga Milk tiene previsto aprovechar esta aprobación para ampliar las colaboraciones con los principales fabricantes de leche de fórmula y promover suplementos y otros productos relacionados en China y en todo el mundo. Al proporcionar información precisa sobre los beneficios de Bifidobacterium infantis M-63 a los consumidores y socios, Morinaga Milk se propone mejorar la salud y la nutrición de las personas en todo el mundo.
Acerca de Morinaga Milk Industry
Morinaga Milk Industry Co., Ltd. es una de las principales empresas de productos lácteos de Japón, con más de un siglo de historia en el aprovechamiento de las propiedades nutricionales de los productos lácteos y los ingredientes funcionales. Morinaga Milk es también un importante fabricante mundial de probióticos que destaca por su tecnología innovadora y ofrece una línea premium de probióticos e ingredientes funcionales en todo el mundo. Desde los años sesenta, Morinaga Milk se ha dedicado a investigar la seguridad, los beneficios funcionales para la salud y los mecanismos de acción de las bifidobacterias probióticas para comprender mejor su papel en el mantenimiento de la salud humana. Para más información sobre los probióticos Morinaga Human-Residential Bifidobacteria (HRB), visítenos en https://morinagamilk-ingredients.com/.
El texto original en el idioma fuente de este comunicado es la versión oficial autorizada. Las traducciones solo se suministran como adaptación y deben cotejarse con el texto en el idioma fuente, que es la única versión del texto que tendrá un efecto legal.
Contacts
Morinaga Milk Industry Co., Ltd.
Mitsunori Watanabe / Kazuaki Kajikawa, Departamento de relaciones públicas y relaciones con los inversores
Junichi Minami / Chyn Boon Wong, División internacional
Correo electrónico: interntl-pr@morinagamilk.co.jp
Morinaga Milk, sitio web: https://www.morinagamilk.co.jp/english/