Mainstay Medical annonce la publication de la première étude sur la neuromodulation pour la lombalgie avec un suivi de 5 ans
Mainstay Medical annonce la publication de la première étude sur la neuromodulation pour la lombalgie avec un suivi de 5 ans
L'étude révolutionnaire ReActiv8-B confirme l'efficacité, l'innocuité et la durabilité à long terme de la neurostimulation restauratrice ReActiv8® TM pour le traitement de la lombalgie chronique incurable
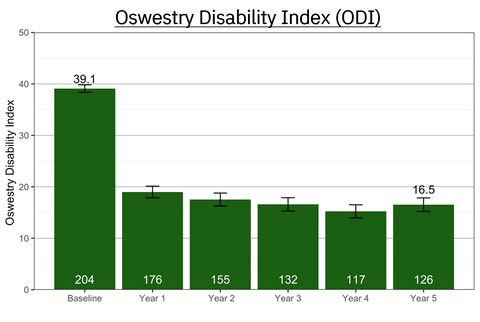
DUBLIN--(BUSINESS WIRE)--Mainstay Medical Holdings plc a annoncé aujourd'hui la publication des résultats du suivi à 5 ans de l'essai randomisé en double aveugle de ReActiv8-B, contrôlé par simulation. Cent vingt-six patients ont achevé le suivi à cinq ans, et les données publiées indiquent clairement que la neurostimulation restauratrice ReActiv8® est un traitement à long terme, efficace, durable et sûr. ReActiv8 est le seul traitement restaurateur pour les patients souffrant d'une lombalgie chronique mécanique non chirurgicale, associée à un dysfonctionnement du muscle multifide.
La publication est disponible à cette adresse :
https://www.sciencedirect.com/science/article/pii/S1094715924000552
Dans le cadre de l'étude ReActiv8-B, plusieurs patients se sont vu retirer leurs implants en raison de douleurs dorsales. Ces retraits réussis indiquent un mécanisme restaurateur, et le traitement ne montre aucun signe d`'une perte d'efficacité généralement observée avec les traitements palliatifs.
Le Dr Chris Gilligan, Chief Medical Officer et Chief Quality Officer au Robert Wood Johnson University Hospital, a déclaré : « Les résultats à long terme et durables de cette étude pour les patients sont sans précédent dans le domaine de la neuromodulation. Il s'agit véritablement d'un traitement unique, restaurateur par nature, et qui ne présente aucune des pertes d'efficacité observées avec d'autres traitements dans notre domaine. Grâce aux résultats publiés sur 5 ans, nous ne sommes plus limités à des traitements temporaires ou palliatifs pour nos patients. ReActiv8 transforme la façon dont nous traitons les patients sélectionnés correctement ».
Jason Hannon, CEO de Mainstay Medical , a déclaré : « Nous sommes fiers de posséder le seul dispositif disponible dans le commerce doté d'un profil de sécurité solide et soumis à un examen à long terme évalué par des pairs qui soutiennent la guérison de cette population de patients gravement atteinte. Nous nous réjouissons de partager ces données avec nos clients médecins et leurs patients, et de les utiliser pour inciter les organismes de gestion des soins aux États-Unis à élargir l'accès des assurances commerciales à ce traitement extraordinaire ».
À propos de ReActiv8®
ReActiv8 est un dispositif médical implantable, conçu pour le traitement des adultes souffrant de lombalgie chronique incurable associée à un dysfonctionnement du muscle multifide. Le dysfonctionnement du muscle multifide peut être diagnostiqué par imagerie ou par des tests physiologiques chez les adultes pour qui les traitements ont échoué, notamment les analgésiques et la physiothérapie, et pour qui la chirurgie rachidienne n’est pas recommandée. ReActiv8 a obtenu des autorisations réglementaires dans plusieurs zones géographiques. Le dispositif est disponible dans l’Espace économique européen, en Australie, au Royaume-Uni et aux États-Unis.
À propos de Mainstay Medical
Mainstay Medical est une entreprise de dispositifs médicaux axée sur la commercialisation de son système innovant de neurostimulation restauratrice implantable, le ReActiv8, pour les personnes souffrant de lombalgie chronique mécanique invalidante. Le siège de Mainstay Medical se trouve à Dublin, en Irlande, et l'entreprise possède des filiales en Irlande, aux États-Unis, en Australie, en Allemagne et aux Pays-Bas.
Pour plus de détails : www.mainstaymedical.com .
Déclarations prospectives de Mainstay
Toutes les déclarations contenues dans cette annonce, autres que les déclarations de faits historiques, sont ou peuvent être considérées comme des déclarations prospectives. Ces déclarations prospectives peuvent inclure, sans limitation, des déclarations concernant les intentions, les convictions ou les attentes actuelles de la Société concernant, entre autres, les résultats cliniques, les efforts commerciaux et les performances, les études et les résultats de la recherche de la Société, sa situation financière, ses stratégies de financement, la conception et le développement de produits de la Société, son portefeuille de propriété intellectuelle et son champ d’application, les demandes et approbations réglementaires et les modalités de remboursement.
Les déclarations prévisionnelles impliquent des risques et des incertitudes et ne constituent pas des garanties de performance future. Les résultats réels peuvent différer matériellement de ceux décrits ou suggérés par les déclarations prévisionnelles. Un certain nombre de facteurs pourraient entraîner des résultats et des développements sensiblement différents de ceux exprimés ou sous-entendus dans les déclarations prévisionnelles du présent document, y compris, mais sans s'y limiter, les risques et incertitudes inclus dans le rapport annuel de la société pour l'exercice clos le 31 décembre 2022, qui doit être lu conjointement avec les informations publiques de la société (disponibles sur le site web de la société ( www.mainstaymedical.com )). The forward-looking statements herein speak only as of the date of this announcement.
Le texte du communiqué issu d’une traduction ne doit d’aucune manière être considéré comme officiel. La seule version du communiqué qui fasse foi est celle du communiqué dans sa langue d’origine. La traduction devra toujours être confrontée au texte source, qui fera jurisprudence.
Contacts
Relations publiques et demandes concernant les relations investisseurs, Mainstay :
L ifeSci Advisors, LLC
Brian Ritchie
Tél. : + 1 (212) 915-2578
E-mail : britchie@lifesciadvisors.com
FTI Consulting (Irlande)
Jonathan Neilan ou Patrick Berkery
Tél. : +353 86 602 5988
E-mail : mainstay@fticonsulting.com
Mainstay Medical
Communication institutionnelle
E-mail : Media@mainstaymedical.com