DANVERS, Massachusetts--(BUSINESS WIRE)--Abiomed (Nasdaq: ABMD) gibt bekannt, dass die US-amerikanische Arzneimittelbehörde FDA die Zulassung vor der Markteinführung (PMA), die höchste Zulassungsstufe der FDA, für Impella RP Flex mit SmartAssist zur Behandlung von Rechtsherzinsuffizienz bis zu 14 Tagen erteilt und das Produkt damit als sicher und wirkungsvoll bestätigt hat. Impella RP Flex wird über die interne Jugularvene (IJ) implantiert und ermöglicht auf diese Weise Patientenmobilität, während die integrierte Dual-Sensor-Technologie das Patientenmanagement optimiert.
Die Impella-RP-Plattform umfasst die kleinsten mechanischen perkutanen Rechtsherz-Kreislaufunterstützungssysteme (MCS) der Welt, die bei Patienten eine Wiederherstellung der nativen Herzfunktion ermöglichen sollen. Sie erfordern keinen extrakorporalen Blutkreislauf und sind bislang die einzigen MCS-Technologien mit FDA-PMA-Indikationen zur Behandlung von Rechtsherzinsuffizienz.
Wichtige klinische Vorteile von Impella RP Flex:
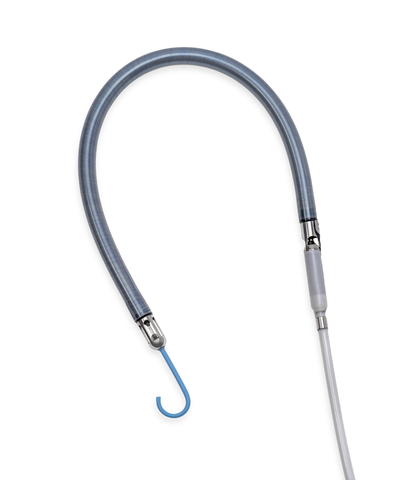
- Venöser Zugang über die interne Jugularvene (IJ) und Dauerkatheter der Größe 11 French (Fr), der Patientenmobilität ermöglicht
- Fortschrittliche flexible Kanüle dank unterstützendem Führungsdraht, der die Einführung und Bereitstellung der Pumpe erleichtert
- SmartAssist-Dual-Sensor-Technologie mit Impella Connect, die fortschrittliche Messgrößen zur Unterstützung von Pumpen-Management und Weaning bietet
- Heparin-freie Reinigung, was das Antikoagulanzien-Management durch die Verwendung von Natriumhydrogenkarbonat vereinfacht, insbesondere bei Patienten, bei denen Heparin aufgrund von Heparin-Unverträglichkeit oder Blutung bedenklich ist
„Impella RP Flex beweist Abiomeds fortlaufendes Engagement für die Verbesserung der Überlebensrate und Wiederherstellung der nativen Herzfunktion von Patienten“, sagte Mark B. Anderson, MD, Chairman der Abteilung für Herzchirurgie und Herz- und Thorax-Chirurg an der Herz- und Gefäßklinik bei HUMC/Hackensack Meridian Health.
Die frühe Erkennung von Rechtsherzinsuffizienz oder rechtsventrikulären Dysfunktion und die frühzeitige Verwendung von Impella RP sind mit wesentlich höheren Überlebensraten assoziiert. Im Journal of Cardiac Failure und Journal of American College of Cardiology veröffentlichte Studien zeigen, dass bei 37 Prozent der Patienten mit kardiogenem AMI-Schock (AMICS) eine Rechtsherz-Dysfunktion vorliegt (Lala et al.) und dass diese mit einem dreimal höheren Mortalitätsrisiko verbunden ist (Mehta et al.). Im Journal of Heart and Lung Transplantation veröffentlichte Ergebnisse zeigen, dass Patienten, die in den ersten 48 Stunden nach dem Eintreten eines kardiogenen Schocks die Unterstützung von Impella RP erhielten, eine wesentlich höhere Überlebensrate hatten als Patienten mit verzögerter Rechtsherz-Unterstützung (73 % vs. 14 %, p<0,001, Anderson et al.).
„Die Komplexität von rechtsventrikulärem Herzversagen hat dazu geführt, dass Patienten unzulänglich diagnostiziert und behandelt werden“, sagte Robert Salazar, MD, interventioneller Kardiologe und Leiter für kardiovaskuläre Forschung am Kingwood Medical Center. „Impella RP Flex ist ein neuartiges Tool, das Ärzten die Flexibilität gibt, diese schwierige Patientengruppe zu behandeln.“
Die FDA-Indikation für die Verwendung von Impella RP Flex mit SmartAssist lautet folgendermaßen:
Das Impella RP Flex mit SmartAssist-System ist für die temporäre rechtsventrikuläre Unterstützung bis zu 14 Tagen bei Patienten indiziert, die eine Körperoberfläche von mindestens 1,5 m2 haben und Rechtsherzinsuffizienz oder Dekompensation nach der Implantation eines linksventrikulären Unterstützungssystems, einem Myokardinfarkt, einer Herztransplantation bzw. einer Operation am offenen Herzen entwickeln.
Impella RP Flex wird in den USA in kontrolliertem Rahmen in diesem Quartal eingeführt.
ÜBER IMPELLA HERZPUMPEN MIT SMARTASSIST
Impella RP® mit SmartAssist ist von der US-amerikanischen Arzneimittelbehörde FDA zur Behandlung von Rechtsherzinsuffizienz oder Dekompensation nach der Implantation eines linksventrikulären Unterstützungssystems, einem Myokardinfarkt, einer Herztransplantation bzw. einer Operation am offenen Herzen zugelassen.
ÜBER ABIOMED
Abiomed (Nasdaq: ABMD) mit Sitz in Danvers, Massachusetts (USA) ist ein führender Anbieter von Medizintechnik zur Kreislaufunterstützung und Oxygenierung. Unsere Produkte entlasten das Herz durch die Verbesserung der Durchblutung und/oder stellen eine ausreichende Sauerstoffversorgung bei Patienten mit Atemwegsversagen sicher. Weitere Informationen finden Sie unter abiomed.com.
ZUKUNFTSGERICHTETE AUSSAGEN
Etwaige zukunftsgerichtete Aussagen unterliegen Risiken und Unwägbarkeiten, beispielsweise denen, die in den regelmäßig von Abiomed bei der US-amerikanischen Börsenaufsicht (SEC) eingereichten Berichten beschrieben sind. Die tatsächlichen Ergebnisse können erheblich von den erwarteten Ergebnissen abweichen.
Die Ausgangssprache, in der der Originaltext veröffentlicht wird, ist die offizielle und autorisierte Version. Übersetzungen werden zur besseren Verständigung mitgeliefert. Nur die Sprachversion, die im Original veröffentlicht wurde, ist rechtsgültig. Gleichen Sie deshalb Übersetzungen mit der originalen Sprachversion der Veröffentlichung ab.